La degeneración macular relacionada con la edad (DME), o senil, es una de las principales causas de ceguera en los mayores de 60 años. Alrededor del 90% de pacientes con DME padecen del tipo “seco”, para el que aún no existe una terapia aprobada.
Así pues, la carrera para hallar una cura ha empezado. El potencial es enorme, pues los productos para tratar el número de pacientes del tipo “húmedo”, que es menor, representan un mercado de $5.000 millones de dólares anuales.
La compañía Cell Cure Neurosciences, con sede en Jerusalén, ha entrado al mercado con un tratamiento de células epiteliales pigmentarias retinales humanas inyectables, que hacen de “ayudantes” esenciales para las células fotoreceptoras del ojo. Son producidas a partir células madre pluripotentes gracias a una tecnología exclusiva de la compañía.
El director ejecutivo de ésta, Charles Irving, explica que el epitelio pigmentario retinal se deteriora con la edad y no proporciona a los fotoreceptores los nutrientes y pigmentos necesarios para funcionar.
“Las células fotoreceptoras pueden vivir un poco más tiempo por sí mismas antes de morir, y eso es irreversible”, dijo a ISRAEL21c. “Nuestro objetivo es facilitar, por primera vez, trasplantes con nuevo epitelio pigmentario retinal de modo que podamos salvar los fotoreceptores que aún no hayan muerto y detener así el avance de la enfermedad”.
Irving compara la degeneración macular en la retina con un incendio en un bosque. El daño puede aceptarse hasta que llegue a las afueras de éste, que en este caso es la fóvea de la mácula, que es diminuta.
“Si la enfermedad llega a la fóvea, se pierde esencialmente la visión central y los colores,” dijo Irving. «Queremos detener el ‘incendio’ antes de que llegue a la fóvea, lo que hacemos por medio de células jóvenes no susceptibles al envejecimiento”.
Pruebas clínicas
OpRegen, producto de Cell Cure Neurosciences, está siendo sometido a pruebas clínicas en el Centro Médico Universitario Hadassah, de Jerusalén, para ver si es idóneo para pacientes con degeneración macular avanzada. La compañía obtuvo aprobación por la vía rápida por parte de la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) para llevar a cabo nuevas pruebas en ese país.
La prueba se realiza en cuatro grupos compuestos de 15 pacientes: los tres primeros recibieron una dosis baja de OpRegen, los tres siguientes, media, y el tercer grupo, la más alta. En el último grupo, que también será reclutado en Estados Unidos a comienzos del próximo año, seis pacientes con DME seca más leve recibirán la dosis más alta para probar así la eficacia de la medicina en una fase temprana.
“Estos estudios iniciales son para mostrar que no se produce ningún daño al introducir nuevas células en la retina y que van a injertarse adecuadamente y a organizarse por su cuenta para apoyar a las células fotoreceptoras”, dijo Irving. “Los estudios siguientes determinarán la eficacia para detener el avance de la enfermedad”.
La habilidad de las células para organizarse solas —probada en estudios con animales realizados por la compañía— es fundamental para entender el carácter único del enfoque de Cell Cure en medicina regenerativa.
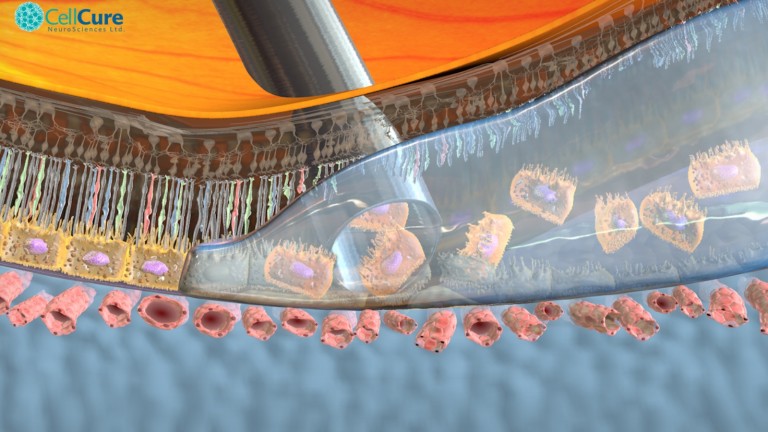
El enfoque experimental más común consiste en organizar el reemplazo de células epiteliales pigmentarias retinales en un parche, para lo cual se requiere una cirugía que exige capacitación especial. OpRegen, en cambio, se inyecta en suspensión en un procedimiento corto, que se realiza una sola vez.
La terapia celular tiene un potencial más amplio que los tratamientos biológicos que se están probando en la actualidad, dijo Irving. Fármacos como los anticuerpos monoclonales sólo sirven para prolongar la vida de los epitelios pigmentarios retinales envejecidos, en vez de reemplazarlos.
Aun así, según Irving, “estamos en los inicios de una carrera y no tiene por qué haber un ganador solamente. No hay ninguna terapia aprobada por el momento, así que hay espacio para otros”.
Otros dispositivos
Fundada en 2005, Cell Cure tiene 25 empleados. El jefe científico, el doctor Benjamin Reubinoff, fue uno de los primeros en el mundo en derivar células madre embrionarias y es un experto en su uso en medicina regenerativa. Los tres principales accionistas de la firma son las compañías BioTime, estadounidense, y Hadasit Bio-Holdings y Teva Pharmaceuticals, ambas israelíes.
La comercialización de OpRegen depende de los resultados del estudio actual, de la aprobación para estudios de eficacia posteriores y de apoyo financiero. Cell Cure ha recibido ayuda anual por unos $9,6 millones de dólares de la Autoridad de Innovación de Israel (antes conocida como la Oficina del Científico Jefe) del Ministerio de Economía e Industria.
Otros dispositivos para DME, todos hechos en Israel, son ForeseeHome, de Notal Vision, el primero aprobado por la FDA para monitorear en casa si hay cambios de tipo seco a húmedo; VisionCare Ophthalmic Technologies, que presenta un implante telescópico para pacientes en la fase final de la enfermedad; y las prótesis artificiales retinales de Nano-Retina, desarrolladas en la actualidad en colaboración con un laboratorio en el estado de Texas, en Estados Unidos.
Para más información, haga clic aquí.


































Comentarios